超音波によるアミロイド線維形成加速現象の機構解明 最終更新:2023年4月12日
I. アミロイド線維の形成過程
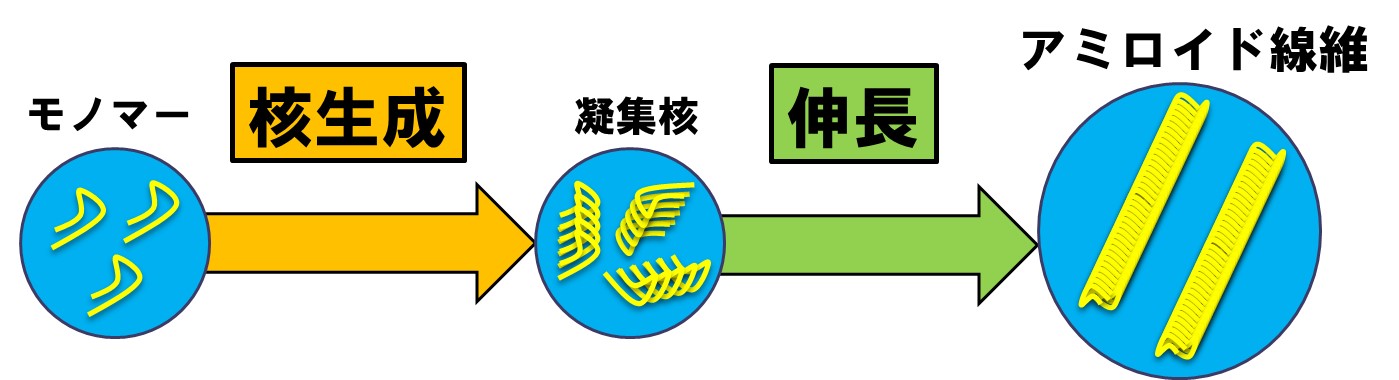
図1. アミロイド線維形成の2段階。核形成段階が時間のかかる遅い反応であるのに対し、線維伸長反応は、核を起点に急速に進行する。
アミロイド線維と難病のページで紹介したように、アミロイド線維の性質を理解し、アミロイド線維が体の中で形成されることを阻止することができれば、アルツハイマー病などの重大な病気の発症を妨げることにつながります。現在、体の中でのアミロイド線維形成を完全に防ぐことはできませんが、アミロイド線維に関連する多くの研究の成果から、なぜ・どのようにしてアミロイド線維が形成されるかの理解が進んできております。アミロイド線維形成反応の特徴として、「核形成」と「線維伸長」という2段階の反応を経て、成熟した線維が形成されることがあげられます(図1)。このうち、核形成反応は、線維ができる起点となる核が形成される反応であり、形成までにとても長い時間を要します。一方、ひとたび核が作られてしまうと、加速的に線維形成反応は進行します。私たちはアミロイド線維形成反応を観察し、その性質やどのようにして形成を防ぐかを考察したいのですが、核形成反応が遅いせいで実験を効率よく実施することが困難でありました。
II. 超音波によるアミロイド形成反応の加速現象
このような状況下で、アミロイド線維の核形成反応を引き起こすために多くの研究者は、蛋白質溶液を激しく撹拌したり振とうしたりすることにより、アミロイド線維形成反応を加速していました。そして、2005年、大阪大学蛋白質研究所・後藤祐児教授のグループは、蛋白質の過飽和溶液に超音波を照射することによりアミロイド線維形成反応が爆発的に加速されることを発見しました(1)。超音波によるアミロイド線維形成反応の加速現象は、アミロイドの研究に有効な手法として研究の手段として用いられていました。超音波は、その音圧(音の大きさ)と周波数(音色)を調整することにより、化学反応に与える影響が大きく異なるということがソノケミストリーの分野の研究から知られているため、メカニズムを解明することで、より有効に超音波の効果を利用することが期待されます。しかしながら、そのメカニズムについての詳細な研究は行われていませんでした。
III. 超音波アミロイド形成加速現象の機構解明
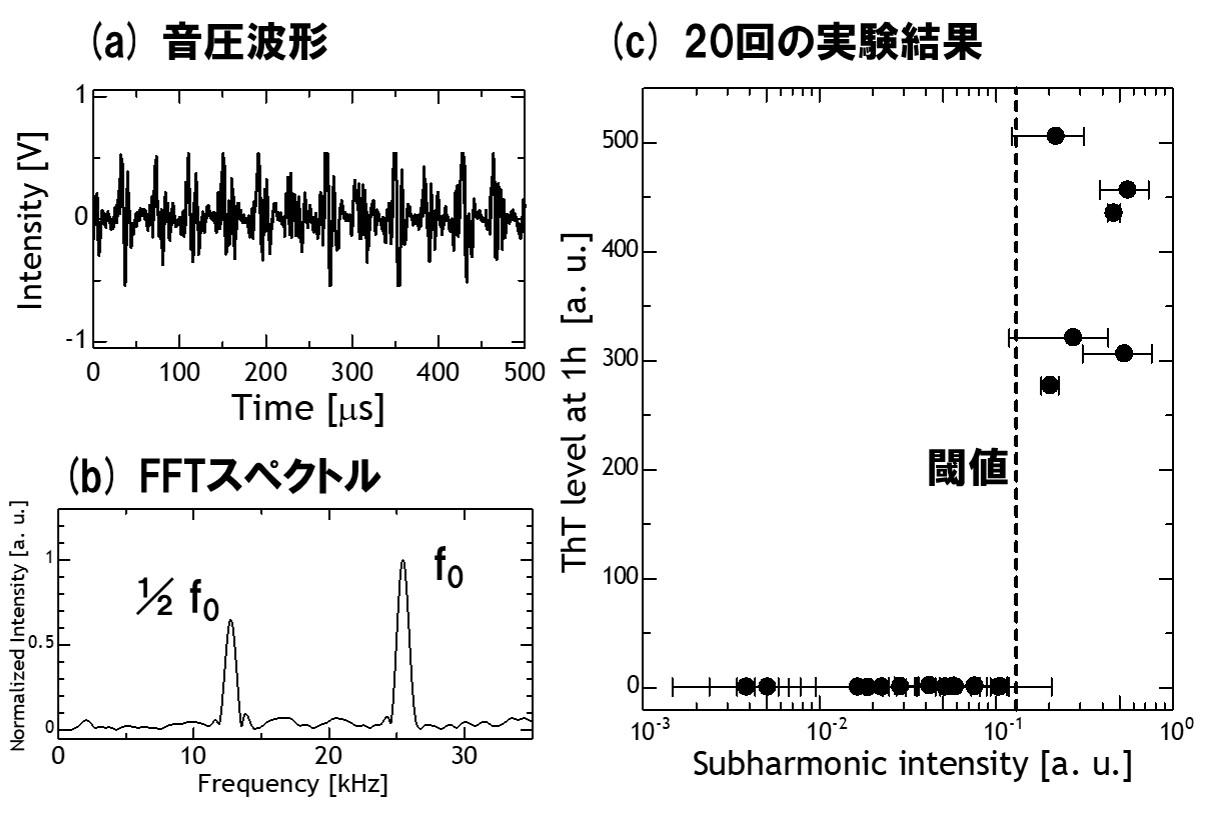
図2. インスリンの超音波音場下でのアミロイド線維形成反応(2)。超音波溶液中の超音波音場の(a)音圧波形と(b)高速Fourier変換(FFT)スペクトル。(c) サブハーモニック強度(横軸)とアミロイド線維量(縦軸)の相関関係。サブハーモニック強度がある閾値を上回った際にアミロイド線維の形成が引き起こされることを示している。
そこで、私たちの研究グループでは、この現象の加速メカニズムに関する研究を行ってきました。まず初めに、インスリンという蛋白質を用いて、超音波を溶液に照射した際に発生する複数の効果の中から支配的な因子を抽出することに取り組みました(2)。超音波を溶液に照射すると、(i) 溶液の温度上昇、(ii) 溶液の撹拌効果、(iii) キャビテーションバブルの発生などの効果が得られます。私たちは、実験を通してこの中で非線形性の強い半径運動を示す過渡的なキャビテーションバブル(transient bubble)が発生する際に、アミロイド線維形成反応の加速が起きることを発見しました。この時には、図2に示すように、超音波音場の周波数成分を詳細に計測・解析し、アミロイド形成反応との関係を調べました。結果として、サブハーモニック(sub-harmonic)と呼ばれる溶液中のキャビテーションバブルの振動が音源となり二次的に放射される周波数成分とアミロイド形成に相関が見つかったため、キャビテーションバブルが加速因子であると結論付けました。
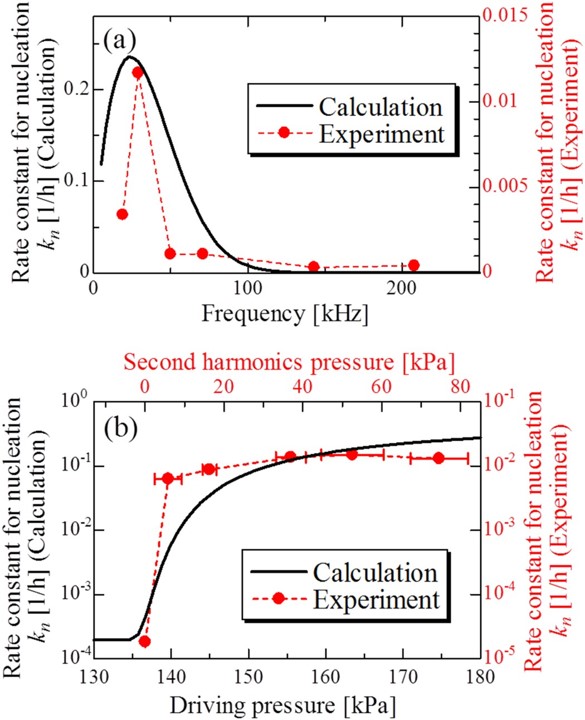
図3. (a) 周波数と(b)音圧の異なる超音波音場下でアミロイドの核が作られる際の速度の変化。
次に、キャビテーションバブルの運動特性を変化させた際に、上述の加速効果がどのように変化するのかを調べました。キャビテーションバブルの運動は、超音波音場の駆動周波数と音圧に強く依存するので、自作の実験装置でこれらのパラメータを変化させた際のアミロイド形成反応の変化を実験的に調査しました(3)。この研究では、アルツハイマー病の原因蛋白質であるアミロイドβペプチドを用いて実験を行いました。実験結果から、超音波による加速効果の程度は、超音波の照射条件により大幅に変化し、特に周波数30 kHz付近でその加速効果が最大になることを発見しました(図3:破線)。この最適周波数において、さらに超音波音圧を調整することにより、最大で核形成反応の反応速度定数を1000倍上昇させることに成功しました(阪大からの紹介記事)。
そして、実験結果から推察される超音波によるアミロイド形成加速モデルを提案しました(図4)。この理論モデルでは、(i) まず、蛋白質溶液に超音波を照射すると溶液中に超音波キャビテーションが発生します(図4(a))。(ii) 次に、発生した気泡は溶液中に気液界面をもたらし、疎水性の高いアミロイドβペプチドを気泡表面に引き付けます。気泡は、超音波の圧力が負圧域にあるときに膨張し、広い範囲にわたって蛋白質分子を吸着します(図4(b))。 (iii) 超音波の圧力が正圧に転じると、気泡は一気に圧壊します。この時、気泡表面に引き付けられた蛋白質分子は気泡の圧壊中心に集められ、局所的に濃度が上昇します。それと同時に、気泡圧壊中心周辺では局所的に温度が上昇し、核形成反応が進行しやすくなります(図4(c))。これらの局所濃度・温度上昇の二重の効果により、アミロイド線維の核形成反応がキャビテーションバブルの半径運動により加速されると考えました。そして、この理論モデルに基づき、気泡の半径運動や統計力学などの理論を用いて、アミロイド核形成の反応速度定数の超音波周波数・音圧依存性の傾向を見積もった結果を図3中に実線で示しています。30 kHzに最適周波数が存在することなどの実験結果の傾向を再現しており、理論モデルの妥当性を支持する結果が得られました。

図4. キャビテーション依存的なアミロイド核形成加速モデル
IV. これからの展開
さらに深くこの現象のメカニズムを理解し、超音波により本来制御が困難なアミロイド線維形成反応を自在に制御することを目指しています。最近では、超音波が単純な溶液の振とうとアミロイド形成反応に及ぼす影響が異なることを詳細に示した論文(4)を発表しました。装置開発・超音波計測・蛋白質を用いた実験・理論計算などが様々な要素が複合しており、将来的に臨床診断等につながる可能性のあるおもしろい研究テーマです!
* 参考文献
(1) Y. Ohhashi et al., "Ultrasonication-induced amyloid fibril formation of β2-microglobulin", J. Biol. Chem. 280, 32843-32848 (2005).
(2) K. Nakajima et al., "Drastic acceleration of fibrillation of insulin by transient cavitation bubble", Ultrason. Sonochem. 36, 206-211 (2017).
(3) K. Nakajima et al., "Nucleus factory on cavitation bubble for amyloid β fibril", Sci. Rep. 6, 22015 (2016).
(4) K. Nakajima and H. Toda et al., "Half-time heat map reveals ultrasonic effects on morphology and kinetics of amyloidogenic aggregation reaction", ACS Chem. Neurosci. 12, 3456-3466 (2021).
戻る